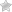Обследования при атеросклерозе аорты:
- общие анализы крови, мочи.
- Биохимические исследования крови: креатинин, мочевина, ХО, ТГ, ЛПВП, ЛПНП, лептин, ПИ, фибриноген, ренин, ангиотензин, альдостерон, кортизол, адреналин, норадреналин, АКТГ, ТТГ, калий, натрий, хлориды.
- ЭКГ, ХМ-АД
- ЭхоКГ.
- Рентгенография сердца.
- УЗДГ сердца, сосудов, почек.
- Аортография, КАП
- Офтальмолог: глазное дно.
C. Bялoв, A. Epмoлoв, C. Чopбинcкaя, E. Чepниeнкo, Т. Bacинa, B. Kyзнeцoв
Локальное отсутствие медии в стенке аорты приводит к развитию аневризм синуса Valsalva. Эти аневризмы могут быть случайными находками при ЭхоКГ. Аневризмы могут прорываться в смежные камеры сердца, чаще всего в ПП, ПЖ или МЖП, и сдавливать рядом расположенные структуры. Парастернальная и апикальная позиции по длинной оси помогают дифференцировать эти аневризмы от аневризм мембранозной части МЖП. Аневризма синуса Valsalva локализуется в аортальной части ЛК, тогда как аневризма мембранозной части МЖП расположена со стороны желудочков. Эти аневризмы можно четко отличить, используя ЧПЭхоКГ и ТТЭхоКГ.
Естественное течение аневризм синуса Valsalva изучено не до конца, однако установлено, что они с высокой вероятностью связаны с эндокардитом, фатальным разрывом, эмболиями и появлением соустий между камерами сердца. Хирургическое лечение строго показано при разрывах аневризм, приводящих к появлению шунта слева направо. Вопрос о пластике неосложненных аневризм решается индивидуально.
При рутинной ТТЭхоКГ у пожилых людей часто визуализируются атеросклеротические бляшки и их фрагменты. Бляшки в Ао обычно имеют неправильную форму и подвижны. В рамках исследования SPARC (Stroke Prevention Assessment of Risk in a Community) бессимптомным больным выполняли ЧПЭхоКГ. В этом исследовании возраст, курение в анамнезе и САА были независимо связаны с атеросклерозом Ао, и фрагменты атеросклеротических бляшек в Ао часто определяли у больных с эмболиями. Изъязвленные бляшки в дуге Ао были обнаружены у 26% из 239 больных с цереброваскулярными событиями и только у 5% из 261 пациента без цереброваскулярной патологии.
Предварительные результаты свидетельствуют, что длительная варфариновая гипокоагуляция эффективна при атеросклерозе для уменьшения вероятности эмболических осложнений; при рецидивирующих эмболиях на фоне гипокоагуляции показано хирургическое удаление бляшек.
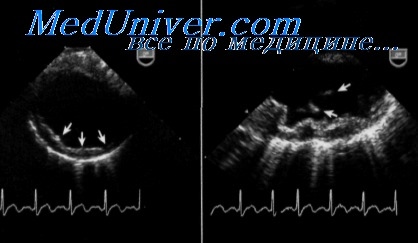
Несмотря на то что у большинства больных с расслоением аорты она расширена при визуализации в В-режнме ЭхоКГ, при ТТЭхоКГ обнаружить расслоение аорты трудно; кроме того, при ТТЭхоКГ невозможно визуализировать нисходящий отдел Ао. При отсутствии данных о расслоении аорты или недостаточно оптимальной визуализации требуется дополнительное обследование.
При ЧПЭхоКГ проксимальное расслоение Ао отображается хорошо. При этом можно полностью визуализировать грудной отдел аорты вследствие его близкого расположения к пищеводу. При горизонтальной чреспищеводной позиции может быть не видна дистальная часть восходящей Ао и проксимальная часть дуги Ао из-за интерпозиции трахеи. Однако эту слепую зону можно визуализировать в продольной позиции, благодаря четкому и полному изображению всей аорты ЧПЭхоКГ изменила роль ЭхоКГ в диагностике и лечении расслоения аорты. В IRAD (International Registry of acute Aortic Dissection) опубликованы методы, использованные для диагностики расслоения аорты. У 628 больных с острым расслоением аорты из 13 международных медицинских центров наиболее распространенными методами диагностики расслоения аорты были КТ и ЧПЭхоКГ.
Многоцентровое исследование European Cooperative Study Group of Echocardiography впервые продемонстрировало, что ЧПЭхоКГ даже превосходит КТ и аортографию в диагностике расслоения Ао (чувствительность 99%). Последующие исследования подтвердили высокую диагностическую ценность ЧПЭхоКГ при расслоении Ао. После широкого распространения ЧПЭхоКГ в клинической практике чувствительность ЧПЭхоКГ, по данным IRAI), снизилась до 88% по сравнению с чувствительностью КГ (93%). В настоящее время ЧПЭхоКГ или КТ с контрастированием являются методами выбора при подозрении на расслоение Ао. Диагностическую точность МР’Г оценивали в недостаточном количестве исследований, но ее клиническое значение ограничено длительностью исследования, трудностями наблюдения за больными во время исследования и большим расстоянием места обследования от отделений реанимации и интенсивной терапии.
Интрамуральная гематома предшествует расслоению аорты и часто ассоциирована с артериальной гипертензией и пожилым возрастом. Интрамуральная гематома появляется у 15-20% больных с расслоением аорты и заканчивается расслоением или разрывом Ао у 45% больных . У 34% гематома полностью исчезает, у 12% заканчивается расслоением Ао, у 20% — развитием аневризмы аорты, у 24% — развитием псевдоаневризмы. Интрамуральная гематома хорошо визуализируется при ЧПЭхоКГ, Представляя собой повышение эхоплотности вдоль стенки Ао, соответствующее формированию тромба между интимой и адвентицией. Это изображение необходимо дифференцировать от атсросклсротичсских бляшек в Ао и аортита. Интрамуральная гематома также легко диагностируется при КТ и МРТ. Аортография — наименее ценный метод диагностики интрамуральной гематомы.
Изъязвление атеросклеротической бляшки в аорту может проникать через внутреннюю эластическую мембрану в медию. Это называют пенетрирующей атеросклеротичсской язвой Ао. Такая язва может привести к появлению интрамуральной гематомы, расслоению или разрыву Ао; ее можно заподозрить у больных артериальной гипертензией при болях в груди или спине, напоминающих боли при расслоении аорты. Язвы обычно локализуются в нисходящем отделе аорты. При ЧПЭхоКГ пенетрирующая язва аорты представляет собой кратерообразное или локальное выпячивание атеросклеротически измененной стенки аорты .
При трансторакальной эхокардиографии можно визуализировать аорту: корень, проксимальные отделы восходящего отдела и часть нисходящего отдела за левым предсердием — из проекции по длинной парастернальной оси левого желудочка, а дугу и часть нисходящей аорты — из супрастернального доступа.
Однако более информативна чреспищеводная ЭхоКГ, показанием к выполнению которой является подозрение на заболевание аорты.
В норме аорта определяется как исходящее из левого желудочка полое трубчатое образование с ровными стенками толщиной до 3 мм и диаметром, составляющим: от 2,0 до 3,7 см — в восходящем отделе, не более 2,4 см — в области дуги и от 1,0 до 1,3 см — в нисходящем отделе. При этом систолическая амплитуда движения корня аорты должна быть более 7 мм.
Атеросклероз
Наиболее частой патологией является атеросклероз, который проявляется изменением стенок аорты: локальным или диффузным утолщением и уплотнением, неровностью контура (рис. 8.10).

Рис. 8.10. Признаки атеросклероза аорты. Изображение из парастернальной позиции по длинной оси в В- и М-режимах
На основании выраженности этих изменений определяют степень поражения стенок аорты: легкую, умеренную, тяжелую.
Аневризмы аорты


Рис. 8.11. Аневризма аорты. Изображение в В-режиме из парастернальной позиции по длинной оси в (а) и апикальной пятикамерной позиции (б)
Аневризмы аорты (рис. 8.11) осложняют атеросклеротическое поражение, но могут быть и проявлением других заболеваний, таких как неспецифический аортоартериит, синдром Марфана, сифилитический аортит, медионекроз аорты (болезнь Эрдгейма), а также результатом травм или сопутствующей патологией при врожденных аномалиях, например бикуспидальном аортальном клапане.
Существуют следующие морфологические варианты аневризмы:
- веретенообразная — диффузное расширение сегмента аорты;
- мешковидная — расширение части окружности аорты в виде выпячивания.
Прямым эхокардиографическим признаком аневризмы аорты является значимое, более чем в два раза, расширение просвета аорты. Характерно снижение пульсации стенок. Могут выявляться пристеночно расположенные тромбы.
Расслоение (диссекция) аорты
Расслоение (диссекция) аорты также может быть диагностировано при трансторакальной ЭхоКГ и ЧПЭхоКГ. Чувствительность этих методов при данной патологии составляет 80 и 94%, специфичность — 95 и 98% соответственно, что сопоставимо с аналогичными показателями компьютерной томографии — 83 и 100%.
По классификации De Bakey различают следующие 3 типа диссекции аорты в зависимости от места расположения отслоившейся интимы:
- тип I — в восходящей аорте, дуге и нисходящем отделе аорты;
- тип II — в восходящей аорте;
- тип III — в нисходящей аорте.
Основным признаком диссекции аорты при ЭхоКГ является дополнительный контур стенки сосуда, который делит сосуд на две части (рис. 8.12).

Рис. 8.12. Расслаивающаяся аневризма аорты
При разрыве аневризмы визуализируется нарушение целостности ее стенки с отслойкой интимы, определяемой как линейное подвижное, флотирующее, образование в просвете аорты — дефект стенки аневризмы. При недостаточности аортального клапана существует возможность перехода разрыва аневризмы на аортальное кольцо, синусы Вальсальвы, брахиоцефальные сосуды, пролапс отслоенной интимы в полость левого желудочка.
Иногда можно увидеть гематому, располагающуюся около контура аорты зитивных тромботических масс.
Специфическими для разрыва аневризмы признаками считают также аортальную недостаточность, выпот в перикардиальной полости, реже — выпот в плевральной полости.
При исследовании расслаивающейся аневризмы аорты определяют не только наличие ее признаков, но и место начала отслойки интимы, ее распространенность, а также указывают выраженность аортальной регургитации.
Аневризма синусов Вальсальвы
Аневризма синусов Вальсальвы, характеризующаяся выпячиванием стенки одного из синусов (их названия соответствуют створкам аортального клапана — левый коронарный, правый коронарный, некоронарный) в расположенную рядом сердечную камеру, обычно является врожденной аномалией (например, при синдроме Марфана), обусловленной слабостью соединения аортальной стенки с фиброзным кольцом клапана, хотя может регистрироваться при аорто-артериите или надклапанном стенозе аорты.
Основная морфологическая форма аневризмы синусов Вальсальвы — изолированная в сочетании с другими дефектами (дефектом перегородки, открытым артериальным протоком, коарктацией аорты, бикуспидальным аортальным клапаном и пр.).
Эхокардиографическим признаком данной патологии является мешковидное выпячивание стенки синуса в одну из полостей сердца: правого — в правое предсердие или выходной отдел правого желудочка, левого — в левое предсердие, некоронарного — в правое предсердие или выходной отдел правого желудочка.
При разрыве синуса на эхокардиограмме, выполненной из парастернального доступа в проекции по короткой оси на уровне аорты, визуализируются как сам перерыв эхосигнала в зоне аневризматического мешка (одиночный или множественный), так и признаки объемной перегрузки той камеры, повреждение правого коронарного синуса, наиболее редко — левого синуса.
При допплерографии и ЦДК регистрируют турбулентный поток крови в соответствующей полости.
Отмечено, что у детей возможно обнаружение дилатации синусов Вальсальвы, чаще некоронарного, при которой расширение синуса не достигает степени аневризмы. Длительное наблюдение таких пациентов указывает на возможность доброкачественного характера этой патологии и спонтанного ее исчезновения по мере роста ребенка.
Дилатация аорты
Дилатация аорты является характерным признаком дисплазии соединительной ткани и выявляется при синдромах Марфана (рис. 8.14),
Элерса-Данлоса и др. В этом случае одновременно определяются пролапс митрального клапана и дополнительные трабекулы в полости левого желудочка, реже — дилатация ствола легочной артерии и др.
При отсутствии перечисленных синдромов следует оценить возможность других причин дилатации аорты — постстенотической дилатации, артериальной гипертензии, аортита, медионекроза. Об идиопатической дилатации аорты можно говорить только после скрупулезного исследования, исключив все перечисленное выше.

Рис. 8.14. Дилатация аорты при синдроме Марфана
Поделиться «Болезни аорты сердца — эхокардиография»